In einer aktuellen Studie mit Mäusen, Labor-grown menschlichen retinalen Zellen und Proben von Patienten der Johns Hopkins Medicine Wissenschaftler sagen, Sie fanden Hinweise auf einen neuen Signalweg, die dazu beitragen kann zu einer degeneration der lichtempfindlichen Gewebes an der Rückseite des Auges. Die Ergebnisse, Sie kommen zu dem Schluss, bringen die Wissenschaftler ein Schritt näher an der Entwicklung neuer Medikamente eine zentrale vision zerstören Komplikation von diabetes, wirkt sich auf schätzungsweise 750,000 Amerikaner.
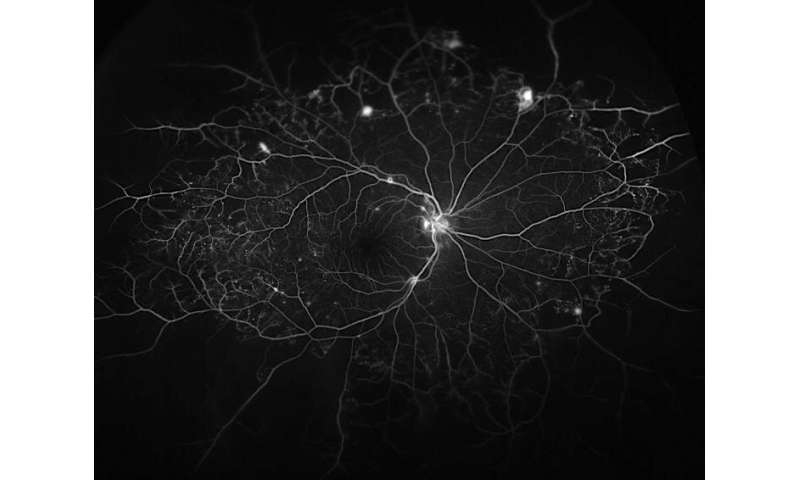
Die Johns Hopkins research-team konzentriert sich auf das diabetische Makulaödem, eine form der Schwellung und Entzündung, die Auftritt, in der Menschen mit diabetes, wenn Blutgefäße im Auge Leck Ihre Flüssigkeiten in dem Teil der Netzhaut, der steuert die detaillierte vision.
Aktuelle Therapien für diese Krankheit blockiert das protein VEGF, das dazu beiträgt, die abnorme Wachstum von Blutgefäßen. Jedoch, da die Behandlung nicht ausreichend ist für mehr als die Hälfte der Patienten mit diabetischen Makulaödem, Forscher haben lange vermutet, dass weitere Faktoren-Laufwerk Verlust des Sehvermögens bei diesen Patienten.
In der neuen Studie der Johns Hopkins Forscher sagen, Sie fanden überzeugende Beweise, dass angiopoietin-like 4 spielen bei der Makula-ödem. Die signaling protein ist bereits gut bekannt, ein Blutgefäß-Wachstumsfaktor mit Rollen Herzerkrankungen, Krebs und metabolische Krankheiten, welche diabetes ist eine.
Ein Bericht über die Ergebnisse wurde veröffentlicht Sept. 23 im Journal of Clinical Investigation”.
Akrit Sodhi, M. D., Ph. D., associate professor für Augenheilkunde an der Johns Hopkins University School of Medicine und der Johns Hopkins Wilmer Eye Institute, in Zusammenarbeit mit Silvia Montaner, Ph. D., M. P. H., an der University of Maryland, führte das Forschungsteam und war fasziniert von angiopoietin-like 4, nach der Feststellung, in früheren Studien, die erhöhte Niveaus dieses proteins in den Augen der Menschen mit einer Vielzahl von vision-Erkrankungen.
In der neuen Studie Sodhi und sein team fanden, dass angiopoietin-like 4 wirkt sowohl unabhängig und synergistisch mit VEGF-Aktivität, und Sie identifizierten einen potenziellen Weg, um es zu blockieren.
Die Forscher machten Ihre Entdeckungen, indem Sie menschliche Blutgefäß-Gewebe Zellen, gewachsen im Labor, um niedrige Konzentrationen von VEGF und angiopoietin-like 4. Zu wissen, dass niedrige Niveaus dieser Faktoren einzeln nicht in der Regel erstellen Sie einen Effekt, die Forscher waren überrascht zu finden, dass Sie in Kombination, low-level-VEGF-und low-level-angiopoeitin-wie 4 hatte einen synergistischen Effekt auf vaskuläre Zell-Durchlässigkeit und verdoppelt die Leckage von retinalen Gefäßen bei Mäusen.
“Diese sagten uns, dass Sie unterhalb der Reizschwelle liegender Ebenen der beiden Moleküle, bei denen weder allein genug ist, um etwas zu tun, aber zusammen, Sie produzieren eine große Wirkung”, sagt Sodhi.
Die verstärkende Wirkung führte die Wissenschaftler zu glauben, dass VEGF und angiopoietin-like 4 teilen ein protein-rezeptor in vaskulären Zellen.
Aber ähnliche Experimente zeigten, dass angiopoietin-like 4 erhöht auch die Bildung von Blutgefäßen unabhängig von VEGF. “Dies könnte erklären, warum manche Patienten erleben Verlust der Sehkraft trotz Behandlung mit den aktuellen anti-VEGF-Therapien”, sagt Sodhi.
Um dies zu testen, das team sah, um zu sehen, ob die angiopoietin-like 4 protein gebunden an einem der Rezeptoren VEGF ist in Labor-gewachsenen menschlichen vaskulären Zellen. Sie fanden heraus, dass angiopoietin-like 4 nicht binden den klassischen VEGF-rezeptor, ist ein Ziel der aktuellen anti-VEGF-Medikamente, aber eine andere, weniger studiert man rief neuropilin.
Mit dem neu identifizierten rezeptor, der Forscher suchte weiter um zu erfahren, ob ein Labor-grown version des Rezeptors blockieren könnte angiopoietin-like 4, bevor es war in der Lage zu interagieren mit Blutgefäß-Zellen.
Zu tun, Sie injiziert ein Lösliches fragment des neuropilin-rezeptor in die Augen von Mäusen pharmakologisch behandelt, um imitieren menschliche diabetes, was einen zweifachen Anstieg der retinalen vaskulären Leckage. Die behandelten diabetischen Mäusen zeigte etwa die Hälfte der Blut-Gefäß-Undichtigkeit als Mäuse, die nicht erhalten die Behandlung, ähnlich der diabetischen Mäuse.
Weiter zu erkunden, die neue rezeptor-basierte Behandlung das Potenzial, Wert für die menschlichen Patienten, die Forscher wuchs menschlichen Blutgefäß-Zellen im Labor in flüssigen Proben, die von den Augen der Patienten mit diabetischen Makulaödem, zu replizieren, die Bedingungen und Wachstumsfaktoren finden sich natürlich im inneren des Patienten, die Augen.
Eine Gruppe solcher Zellen ausgesetzt war, der lösliche rezeptor neuropilin. Die Forscher sagen, Sie beobachteten eine deutliche Abnahme in der Diabetes-Makula-ödem-behandelten Zellen mit dem rezeptor im Vergleich zu unbehandelten Zellen.
“Das gibt uns zuversicht, dass dieser Ansatz funktionieren wird, die in menschlichen Augen”, sagt Sodhi, obwohl er warnt, dass die klinische Verwendung von einer Behandlung auf der Basis der Ergebnisse erfordert viele weitere Jahre der Forschung.
Als Nächstes hoffen die Forscher, einen Blick auf die molekularen Wechselwirkungen zwischen angiopoietin-like 4 und den neuropilin-rezeptor. Dabei, sagt Sodhi, die es Ihnen ermöglichen, zu schaffen ein raffiniertes Spiel, die binden können, so viel vision-bedrohlichen angiopoietin-like 4 in das Auge wie möglich.








