Ergebnisse einer neuen Studie unter der Leitung von Prof. Xu Guowang vom Dalian Institute of Chemical Physics (DICP) der chinesischen Akademie der Wissenschaften und Prof. Yang Chunzhang aus dem National Cancer Institute Licht auf die selektive Therapeutika gegen IDH1-mutierte Gliome durch die Ausrichtung auf die Glutathion-Synthese-Weg.
Die Studie wurde veröffentlicht in der Proceedings of the National Academy of Sciences auf Apr. 14. Das Gliom ist die häufigste Art von primären Gehirntumor. Isocitrate dehydrogenase I (IDH1) – mutation ist eine Krebs-assoziierten mutation sehr weit verbreitet bei Patienten mit Gliom.
Obwohl die Onkogene Rolle von IDH1-mutation hat sich gezeigt in mehreren humanen soliden Tumoren, selektive Therapeutika für die IDH1-mutierten malignen Erkrankungen bleiben nicht verfügbar.
Die Forscher gezeigt, dass die Glutathion-de-novo-Synthese spielt eine wesentliche Rolle im IDH1-mutierten Krebszellen. Glutathion-Synthese wurde kontrolliert, indem ein Transkriptionsfaktor NF-E2-related factor 2 (Nrf2), die regelt die gen-expressions für antioxidative Weg.
“Unsere in-vitro-Ergebnisse deuten darauf hin, dass die Unterbrechung des Nrf2-gesteuerte Glutathion-Synthese-pathway stellt synergistische Letalität mit einer neomorphic IDH1-mutation”, sagt Prof. Xu.
Triptolid erstellen, ein diterpenoid-Epoxid aus Tripterygium wilfordii, diente als eine potente Nrf2-inhibitor. “Triptolid erstellen ausgestellt selektive Zytotoxizität an Patienten-abgeleiteten IDH1-mutierte Gliome-Zellen in vitro und in vivo. Darüber hinaus untersuchten wir die Anti-Krebs-Mechanismus von triptolid erstellen.” Yang sagte.
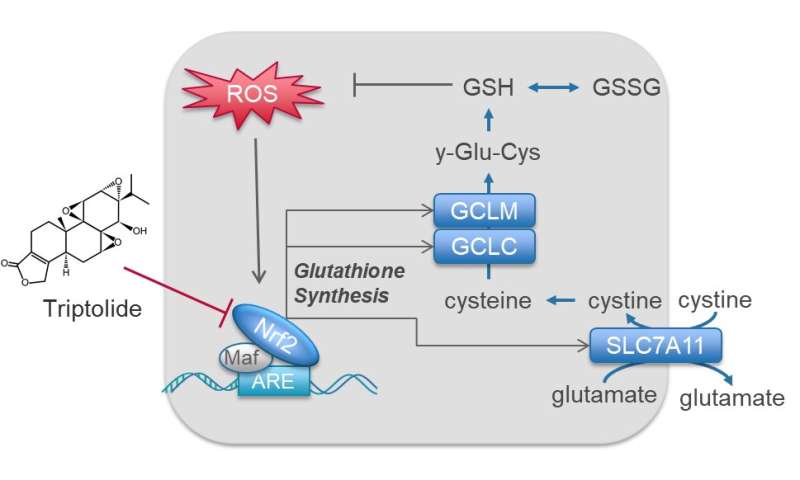
Mechanistisch, triptolid erstellen beeinträchtigt die expression des GCLC, GCLM, und SLC7A11, gestört, die Glutathion-Metabolismus und etablierte synthetische Letalität mit reaktiven Sauerstoff-Spezies (ROS), abgeleitet von IDH1-mutierten neomorphic Aktivität.






